發(fā)布日期:2025-07-03 點擊數(shù):
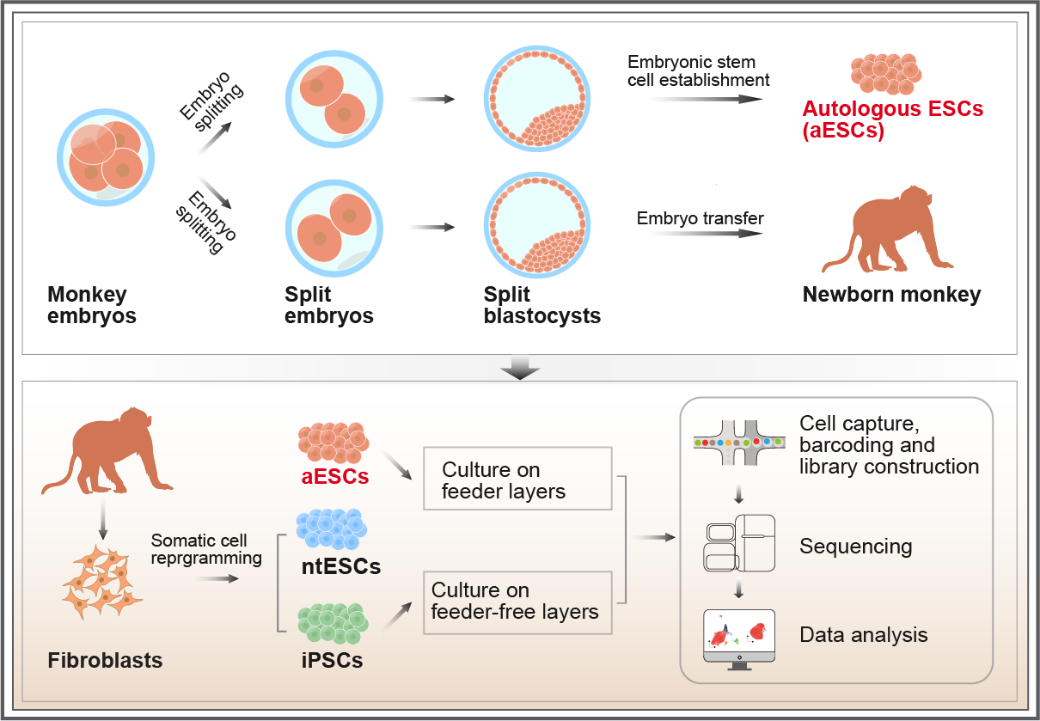
7月1日,昆明理工大學靈長類轉(zhuǎn)化醫(yī)學研究院/省部共建非人靈長類生物醫(yī)學國家重點實驗室、生命科學與技術(shù)學院和西南聯(lián)合研究生院牛昱宇/代紹興/季維智團隊合作在《Nature Communications》雜志上發(fā)表了題為“Production of live monkeys and their genetically matched embryonic stem cells from single embryos”的研究論文。該研究首次利用胚胎分割技術(shù)在維持猴胚胎發(fā)育潛能的同時,成功獲得3只健康猴及其遺傳背景匹配的自體胚胎干細胞(autologous embryonic stem cells, aESCs)。且從同一只猴建立了遺傳背景一致的誘導多能干細胞(induced pluripotent stem cells, iPSCs)和體細胞核移植胚胎干細胞(nuclear transfer embryonic stem cells, ntESCs),首次獲得遺傳背景完全一致的靈長類ESCs、iPSCs和ntESCs。單細胞轉(zhuǎn)錄組分析揭示,相比iPSCs和ntESCs,aESCs可能具有更低的細胞異質(zhì)性、轉(zhuǎn)錄噪音和更高的基因組穩(wěn)定性。

通過體細胞重編程(如誘導重編程、化學重編程和核移植重編程)可獲得與個體遺傳背景匹配的多能干細胞(iPSCs, ntESCs),用于再生醫(yī)學可降低排斥風險,但重編程過程不可避免的增加了潛在的突變壓力和表觀異常風險。胚胎干細胞(embryonic stem cells, ESCs)直接來自于囊胚的內(nèi)細胞團,并不經(jīng)歷重編程過程,在表觀遺傳特征上更加接近自然發(fā)育狀態(tài),但獲取涉及整個胚胎,存在倫理問題。如何在保留胚胎發(fā)育潛能的同時獲得遺傳背景匹配的ESCs?這面臨技術(shù)倫理挑戰(zhàn)。
胚胎分割技術(shù)模擬自然同卵多胞胎形成過程,將單個胚胎分割為多個遺傳匹配的胚胎。該技術(shù)在非人靈長類效率低1,2,人類應用數(shù)據(jù)有限3。研究團隊優(yōu)化了分割策略:在4細胞期(2:2)和8細胞期(3:5)構(gòu)建分割胚胎。分割胚胎囊胚率、發(fā)育時序和譜系標志物表達與對照相當,可同效率產(chǎn)生活體后代或建立ESCs。4細胞期2:2方案中,22對分割胚胎產(chǎn)出1只健康猴及其aESCs。分析發(fā)現(xiàn)源自同一胚胎的兩個分割胚胎上胚層細胞數(shù)差異顯著,可能影響aESC效率。團隊進而采用8細胞期3:5策略:細胞多的胚胎用于移植,細胞少的用于建立aESCs。此方案從23對分割胚胎中獲得2只健康猴及其aESCs(另有1例建立aESCs后孕中期流產(chǎn))。
隨后團隊從其中一只猴獲得遺傳背景匹配的iPSCs和ntESCs。這使團隊能最大程度排除遺傳背景干擾4-6,多維度比較三種干細胞。不同培養(yǎng)條件下單細胞轉(zhuǎn)錄組分析顯示:有飼養(yǎng)層時,iPSCs轉(zhuǎn)錄異質(zhì)性較高,暗示較強分化趨向,而aESCs和ntESCs更相似;無飼養(yǎng)層時,三者異質(zhì)性均降低。相比iPSCs和ntESCs,aESCs轉(zhuǎn)錄組噪音更低,基因組穩(wěn)定性相關(guān)基因表達更顯著。這表明aESCs在細胞異質(zhì)性、轉(zhuǎn)錄組和基因組穩(wěn)定性上可能優(yōu)于iPSCs。考慮到胚胎分割與核移植在倫理和技術(shù)上的差異,aESCs在展現(xiàn)ESCs特征的同時,相比ntESCs具有技術(shù)優(yōu)勢。當然,系統(tǒng)評估三者差異,尤其是體內(nèi)功能表現(xiàn),仍需更多研究。此外,團隊還在人類輔助生殖胚胎上成功建立了分割來源的ESCs,展示了建立人類自體胚胎干細胞的潛力。aESCs能否用于治療,很大程度上取決于建系效率,特別是從少量細胞建系的可行性7, 8。
綜上,本研究不僅開創(chuàng)了從分割胚胎生成自體多能干細胞(aESCs)的新方法,還揭示了aESCs相較于iPSCs和ntESCs的可能潛在優(yōu)勢。并為aESCs 在人類再生醫(yī)學中的進一步應用提供了理論基礎和研究模型。
昆明理工大學靈長類轉(zhuǎn)化醫(yī)學研究院牛昱宇教授、代紹興教授和季維智院士為該研究的共同通訊作者。司晨洋副教授、博士研究生朱然、吳俊模博士、陳枕枕博士為該研究的共同第一作者。該研究得到中國人民解放軍總醫(yī)院第五醫(yī)學中心公彥棟副研究員;昆明理工大學靈長類轉(zhuǎn)化醫(yī)學研究院艾宗勇研究員、尹宇副教授;昆明理工大學靈長類轉(zhuǎn)化醫(yī)學研究院遺傳工程平臺、先進影像平臺、生物信息大數(shù)據(jù)平臺和實驗動物中心的大力幫助。研究受到國家重點研發(fā)計劃和國家自然科學基金等項目的資助。
原文鏈接:https://www.nature.com/articles/s41467-025-60694-5
1. Chan, A.W., T. Dominko, C.M. Luetjens, E. Neuber, C. Martinovich, et al., Clonal propagation of primate offspring by embryo splitting. Science 287, 317-9 (2000).
2. Mitalipov, S.M., R.R. Yeoman, H.C. Kuo, and D.P. Wolf, Monozygotic twinning in rhesus monkeys by manipulation of in vitro-derived embryos. Biol Reprod 66, 1449-55 (2002).
3. Noli, L., Y. Dajani, A. Capalbo, J. Bvumbe, L. Rienzi, et al., Developmental clock compromises human twin model created by embryo splitting. Hum Reprod 30, 2774-84 (2015).
4. Choi, J., S. Lee, W. Mallard, K. Clement, G.M. Tagliazucchi, et al., A comparison of genetically matched cell lines reveals the equivalence of human iPSCs and ESCs. Nat Biotechnol 33, 1173-81 (2015).
5. Zhao, M.T., H. Chen, Q. Liu, N.Y. Shao, N. Sayed, et al., Molecular and functional resemblance of differentiated cells derived from isogenic human iPSCs and SCNT-derived ESCs. Proc Natl Acad Sci U S A 114, E11111-E11120 (2017).
6. Kilpinen, H., A. Goncalves, A. Leha, V. Afzal, K. Alasoo, et al., Common genetic variation drives molecular heterogeneity in human iPSCs. Nature 546, 370-375 (2017).
7. Klimanskaya, I., Y. Chung, S. Becker, S.J. Lu, and R. Lanza, Human embryonic stem cell lines derived from single blastomeres. Nature 444, 481-5 (2006).
8. Chung, Y., I. Klimanskaya, S. Becker, T. Li, M. Maserati, et al., Human embryonic stem cell lines generated without embryo destruction. Cell Stem Cell 2, 113-7 (2008).
